Ciò che siamo non è già scritto e racchiuso nel nostro genoma, ma, come è stato ampiamente dimostrato, è determinato da un processo di interazione dinamica tra il genoma e il nostro ambiente. Le esperienze fatte nell’ambiente quotidiano sarebbero, infatti, in grado di modellare l’attività dei geni, attraverso le cosiddette modificazioni epigenetiche, e quindi le relazioni tra genotipo, fenotipo e ambiente sarebbero governate da simili processi molecolari.
Le esperienze di cui ognuno è protagonista, vengono codificate all’interno del nostro DNA tramite particolari e precisi meccanismi di regolazione dei geni, che entrano in gioco già durante lo sviluppo embrionale.
L’epigenetica è una branca di studi che si occupa dei cambiamenti che influenzano il fenotipo senza alterare il genotipo. Consiste in una serie di vie molecolari attraverso le quali la trascrizione viene alterata, senza però andare a modificare la sequenza di DNA sottostante (la trascrizione è il processo mediante il quale le informazioni contenute nel DNA vengono trascritte per via enzimatica in una molecola complementare di RNA).
Le esposizioni all’ambiente in grado di influenzare i geni sono varie e riguardano il tipo e il livello di nutrienti assunti durante lo sviluppo, le tossine a cui ci si trova esposti e il livello di stress sia nella prima infanzia che negli stadi di sviluppo successivi. Inoltre, studi animali hanno dimostrato come gli effetti dell’esperienza sociale si ripercuotano sulle vie (pathway) epigenetiche che influenzano caratteristiche come la risposta allo stress, l’apprendimento, la memoria e il comportamento riproduttivo.
Le modificazioni epigenetiche possono, a seconda del tipo, incrementare o sopprimere la trascrizione, attraverso una varietà di pathway: la metilazione del DNA, le modificazioni degli istoni e i microRNA (miRNAs). (1)
Metilazione del DNA: La metilazione è considerata come un meccanismo di silenziamento genico.
Per poter iniziare la trascrizione è necessario che il DNA che verrà usato come template sia “accessibile” all’RNA polimerasi e ai fattori di trascrizione. La metilazione del DNA è una modificazione epigenetica che ne altera l’accessibilità senza andare a modificare la sequenza di DNA sottostante.
Quando, all’interno di un gene, compare la coppia di basi C – G, la citosina può essere facilmente metilata dall’azione di un enzima detto DNA Metiltransferasi (DNMTs) che si occupa di aggiungere un gruppo metile a quella citosina (il gruppo è il CH3 – carbonio con 3 atomi di idrogeno).
Quando una sequenza è metilata, non è possibile trascriverla, ovvero non è possibile “leggere” quel gene, che rimane quindi silenziato.
La metilazione del DNA è un processo fondamentale durante lo sviluppo, poiché consente di creare pattern di differenziazione cellulare stabili ed ereditabili.
Durante le rapide fasi di proliferazione e differenziazione cellulare che avvengono nei primi stadi dello sviluppo dell’embrione, è essenziale che il processo di metilazione si verifichi correttamente per la sopravvivenza dell’embrione stesso.
Siccome le cellule embrionali (staminali) possono potenzialmente differenziarsi in qualunque cellula dell’organismo, a seconda della sede in cui si trovano, occorre che diversi geni vengano metilati.
Inattivando alcuni geni e lasciandone altri inalterati, una cellula embrionale entrerà in possesso di uno specifico set genetico che le consentirà di differenziare in un miocardiocita, in un neurone oppure in una cellula epiteliale, pronta per assolvere i suoi compiti nell’organismo formato.
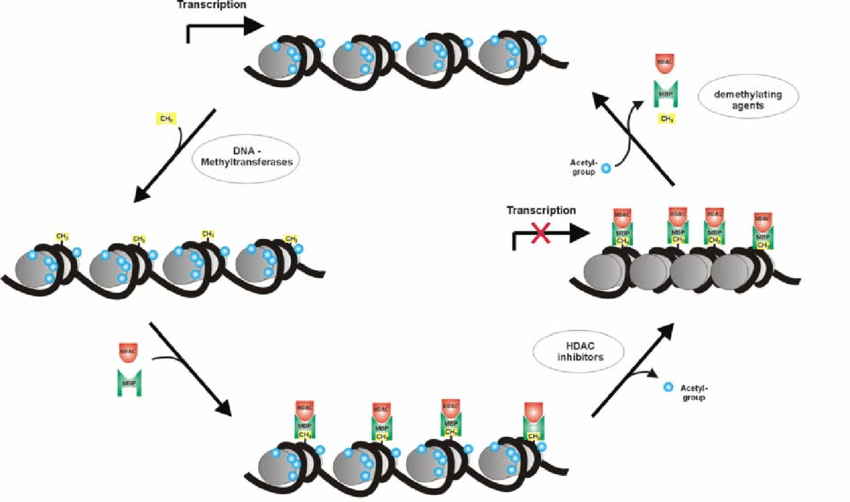
Modificazione degli istoni: L’impacchettamento del DNA all’interno del nucleo della cellula dipende dal grado di condensazione della cromatina ad opera dei nucleosomi, unità fondamentali di cromatina che consistono in DNA impacchettato intorno a un core proteico.
Il core proteico di un nucleosoma è composto da proteine dette istoni. Ne esistono diversi tipi, chiamati H2a, H2b, H3, H4 ecc. Le “code” (estremità N-terminali) degli istoni possono subire diverse modificazioni post-traduzionali, in grado di alterare la struttura della cromatina, rendendola più o meno compatta e quindi più o meno trascrivibile.
Queste modificazioni includono l’acetilazione, la metilazione, l’ubiquitinazione e la fosforilazione. Il tipo e la collocazione della modificazione determinerà l’effetto sulla trascrizione di un dato gene.
Ad esempio, l’acetilazione della lisina nell’istone H3 è tipicamente associata ad una intensa attività trascrizionale, mentre la metilazione dello stesso istone la riduce.
Queste due modificazioni prese ad esempio sono guidate da enzimi tessuto-specifici, che, a seconda della richiesta, aggiungono o rimuovono gruppi acetile o metile dalle “code” degli istoni, rispettivamente incrementandone o riducendone l’attività trascrizionale. Mutazioni che coinvolgono i geni che codificano per questi enzimi possono influenzare profondamente lo sviluppo.
Anche queste modificazioni sono reversibili, non influenzando la sequenza di DNA originale, ma soltanto rendendo la struttura della cromatina “più aperta” o “più chiusa” e quindi rendendo i geni sottostanti “leggibili” o meno.

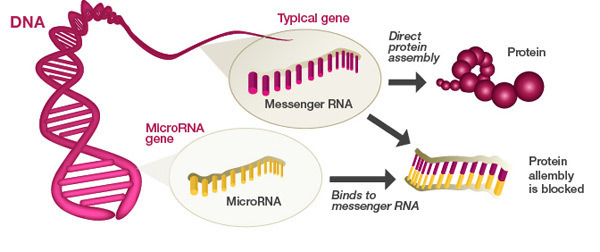
MicroRNA: i microRNA (miRNA) sono piccole molecole di RNA non codificante, in grado di interferire con molecole di RNA messaggero che presentano sequenze complementari a quelle di un dato miRNA, col quale possono appaiarsi. I miRNA riescono a sopprimere l’attività di geni legandosi all’RNA messaggero di molti geni target e a prevenire la traduzione, tagliando l’mRNA o promuovendone la degradazione. Un numero crescente di miRNA è stato identificato per avere specificità riguardo il range di geni target che sono repressi da queste molecole.
L’influenza dell’ambiente. I meccanismi epigenetici conferiscono un alto grado di plasticità e stabilità al pattern di espressione genica di ciascun individuo, tuttavia si pensava che la flessibilità di questi meccanismi (in particolare della metilazione) in risposta ai segnali provenienti dall’ambiente fosse limitata ai primi stadi di sviluppo embrionico.
Invece, è stato ampiamente dimostrato che le differenze individuali nell’espressione genica possono presentarsi a fronte di esperienze individuali ambientali che si verificano durante tutto l’arco della vita, quindi non limitate ai primi contatti con l’ambiente esterno durante l’infanzia.
Negli umani, gli studi sui gemelli monozigoti hanno fornito interessanti risultati riguardo il potenziale della plasticità epigenetica nel guidare divergenze a livello del fenotipo.
Da questi studi, i pattern di metilazione e acetilazione del DNA risultavano altamente concordanti tra gemelli al di sotto dei 28 anni di età, ma divergono significativamente tra gemelli più anziani (oltre 28 anni), portando a speculare che questa divergenza emerga in risposta alle esperienze ambientali uniche di ciascun gemello. Quindi, i cambiamenti epigenetici non hanno luogo solo nei primi stadi di sviluppo, ma anche nel corso della vita adulta, come risposta di adattamento all’ambiente esterno.
Anche le influenze dell’ambiente sociale possono concorrere, durante lo sviluppo, a costruire determinati pattern epigenetici.
Decadi di studi longitudinali e di laboratorio hanno evidenziato l’associazione tra la qualità dell’ambiente sociale e le conseguenze neurobiologiche e comportamentali sugli animali e sugli esseri umani.
In particolare, questi studi indicano che gli effetti epigenetici vengono primariamente indotti dalla qualità dell’interazione madre-figlio e dall’esperienza di incontri sociali agonistici nell’età adulta.
L’impatto epigenetico dei traumi infantili. C’è evidenza crescente che le variazioni epigenetiche possono essere osservate tra individui che hanno sperimentato avversità durante l’infanzia.
La plasticità della metilazione del DNA e delle modificazioni post-traduzionali degli istoni, in risposta alle esperienze sia post-natali che della vita adulta, suggeriscono che i meccanismi epigenetici potrebbero essersi evoluti per permettere agli organismi di adattarsi alle condizioni mutevoli dell’ambiente.
Gli eventi altamente stressanti (lutti, abusi, malattie, traumi) lasciano il segno sia nel fisico che nella psiche, soprattutto su un bambino o un adolescente. Ma gli effetti di questi traumi possono anche essere ereditati e manifestarsi nei discendenti, sotto forma diproblemi di salute fisica o psicologica, patologie psichiatriche e disturbi dello sviluppo.
A dimostrarlo è stato uno studio (2), condotto da un gruppo di ricerca della Tufts University School of Medicine nel Massachusetts e pubblicato su Translational Psychiatry, che conferma come tratti di fragilità nei bambini possano essere collegati ad alterazioni epigenetiche, trasmesse loro dai genitori.
Ciò che viene ereditato non è una sequenza di Dna associata al trauma, ma una variazione di come i geni si esprimono – quindi si manifestano – nel fenotipo.
I ricercatori hanno analizzato, in un gruppo di volontari umani (28 uomini adulti), la relazione fra un trauma del passato e l’eventuale presenza di tali modificazioni epigenetiche.
I ricercatori hanno proposto ai volontari il questionario Adverse Childhood Experiences (Ace), un test con 10 domande che viene usato per rilevare traumi durante l’infanzia e l’adolescenza: fra gli eventi più stressanti sono stati indicati abusi fisici o psicologici, abbandono, mancanza di cure, divorzio dei genitori ecc.
Individuati i traumi, hanno proceduto ad identificare i microRNA (presenti anche nello sperma umano) in quanto alcune evidenze hanno dimostrato che fattori esterni, ad esempio l’abitudine al fumo e l’obesità, possono alterarli. Ma solo oggi arriva la dimostrazione che lo stress possa impattare su tali componenti.
Dai risultati è emerso che i traumi sono collegati ai livelli di due miRNA individuati negli spermatozoi umani, chiamati miR-449 and miR-34.
I volontari che avevano vissuto eventi traumatici particolarmente gravi e protratti nel tempo, presentavano livelli 300 volte più bassi di questi due miRNA rispetto a chi aveva subito traumi minori.
Con studi precedenti su topi, inoltre, i ricercatori avevano mostrato che queste variazioni erano associate ad ansia e a problemi nella socievolezza delle cavie per almeno tre generazioni.
Questi studi confermano che i cambiamenti epigenetici sono stabili ed ereditabili e che lo stress è anch’esso quindi ereditabile. Sarebbe importante tenere in considerazione le modificazioni epigenetiche anche per avere un quadro più chiaro della salute fisica e mentale di un paziente.
Questi cambiamenti, come già ribadito, sono reversibili (a differenza di quelli genetici che alterano le sequenze del Dna) quindi, in via teorica, un giorno si potrebbe essere grado di intervenire per ripristinare i bassi livelli di miRNA negli uomini esposti a traumi estremi.
sources:
(1) Interplay between social experiences and the genome: epigenetic consequences for behavior.
(2) Reduced levels of miRNAs 449 and 34 in sperm of mice and men exposed to early life stress.
[wl_vocabulary][wl_timeline]